∞¥∆∑≈∆þxìÒ
|
||||||||||||||||||||||||||||||
| [∞l±Ì‘u’ì] [±æÓê∆‰À˚Æa∆∑] [±æÓê∆‰À˚π©ë™…Ã] [ ’≤ÿ] | ||||||||||||||||||||||||||||||
| ‰N €…ã∫ …œ∫£Îpƒ´…˙ŒÔø∆ºº”–œÞπ´Àæ | ≤Èø¥‘ìπ´ÀæÀ˘”–Æa∆∑ >> |
SapidyneInstruments Inc. 1995ƒÍ‘⁄√¿á¯Ñì¡¢Æa∆∑ª˘”⁄™öÃÿµƒKinetic Exclusion Assay£®KinExA®£©å£¿˚ºº–g°£KinExA∑÷Œˆ»˝æSÀÆ∆Ωº∞”ŒÎxÝÓëBœýª•◊˜”√£¨≤ªπÃ∂®»Œ∫Œ∑÷◊”°¢≤ªï˛å¶∆Ω∫‚éßÅÌ”∞Ìë°¢õ]”–Ÿ|¡øþw“∆µƒœÞ÷∆°¢ø…“‘ôzúyŒ¥ºÉªØò”∆∑∫ÕÕÍ’˚ºö∞˚£ª“Ú¥Àæþ”–òOåí∑∂á˙É»µƒ…˙ŒÔ∑÷◊”°¢…˙ŒÔΩYòãº∞ÕÍ’˚ºö∞˚Ï`ªÓ∑÷Œˆ∑∂á˙°£◊Ó–¬–ÕÃñKinExA 4000ø…“‘ôzúyºö∞˚£®ÃÏ»ªµƒ∫Õπ§≥êصƒ£©°¢∑«ºÉªØò”∆∑°¢—™«Âò”∆∑£¨–°∑÷◊”µ»µƒœýª•◊˜”√∫Õ”H∫Õ¡¶°£ÀƒÇÄÓw¡£É¶¥Ê∆˜ø…»ðº{Àƒ∑N≤ªÕ¨µƒπÃœýÑ©£¨≤¢ø…≈c∂ýþ_270ÇÄò”∆∑“ª∆÷ß≥÷ÈLïrÈgµƒüo»À÷µ ÿ≤Ÿ◊˜£¨KinExAƒÐâÚúy¡ø…˙¿ÌœýÍPólº˛œ¬µƒœýª•◊˜”√°£
KinExAµƒë™”√£∫
ë™”√“ª°¢KinExA‘⁄CAR-Tºö∞˚÷ŒØü÷–µƒë™”√
“Ú∂ý∑N“ÚÀÿµƒœÞ÷∆£¨◊‘ÛwCAR-Tºö∞˚÷ŒØüÆa∆∑ø…ƒÐ‘⁄ë™”√”⁄ªº’þ«∞Œ¥±ÿƒÐâÚþM––»´≤øÌóƒøµƒôz∂®£¨À˘“‘π§ÀáÚû◊C∑«≥£÷ÿ“™°£π§Àá—–æøº∞Úû◊C±ÿÌöΩY∫œπ§ÀᵃåçÎH«Èõr‘O∂®œý뙵ƒÚû◊C֢¨CAR-Tºö∞˚Æa∆∑π§Àá—–æø‘⁄≤ªîý∞l’𣨵كø«∞ûÈ÷π£¨òIΩÁå¶∫Œ∑Nπ§Àá◊Ó∫√≤¢Œ¥þ_≥…π≤◊R°£“Ú¥À£¨ø…“‘‘⁄Æa∆∑—–∞lþ^≥ú∞‘Á∆⁄≈R¥≤‘áÚûÎA∂ŒÈ_’π≤ªÕ¨≥Ã∂»µƒπ§ÀáÚû◊C—–æø£¨π§ÀáÚû◊CÕÍ≥…∫Û£¨ë™‘⁄ÍPÊIπ§Àá≤ΩÛE‘O÷√ÍPÊIþ^≥Ãøÿ÷∆֢∞òÀú £¨“‘÷∏þCAR-Tºö∞˚Æa∆∑µƒ…˙Æa“ª÷¬–‘°£
CAR-Tºö∞˚÷ŒØüÆa∆∑µƒŸ|¡øøÿ÷∆—–æøº∞ôzúyÌóƒø“ª∞„ë™∞¸¿®£∫ºö∞˚øº∞∆‰¥ÊªÓ¬ °¢ºö∞˚±Ì–Õ°¢CARÍñ–‘¬ ôzúy°¢…˙ŒÔåW–ß¡¶ôzúy£¨üoæ˙ôzúy°¢÷ß‘≠Ûw°¢ü·‘≠/É»∂æÀÿµƒôzúy°¢CAR-Tºö∞˚÷–≤°∂æðdÛwøΩÿê∞’˚∫œµƒôzúyµ»°£»Áπ˚ƒÐâÚôzúyCAR-Tºö∞˚≈cøπ‘≠∑÷◊”µƒ”H∫Õ¡¶£¨“‘º∞CAR-Tºö∞˚…œøπÛwµƒ±Ìþ_¡ø£¨üo“…ï˛Ã·…˝CAR-Tºö∞˚µƒŸ|¡øøÿ÷∆òÀú °£
ƒø«∞ –√Ê…œ≥˝¡ÀKinExAºº–gÕ‚£¨õ]”–∆‰À˚ÃÿÑe”––ßµƒ∑Ω ΩôzúyÕÍ’˚ºö∞˚≈c∑÷◊”Ègµƒ”H∫Õ¡¶£¨∏¸üoèƒ≈–îýºö∞˚…œ∑÷◊”µƒ±Ìþ_¡ø°£KinExAºº–gø…“‘ôzúyºö∞˚≈c∑÷◊”Ègµƒ”H∫Õ¡¶£¨≤¢«“ø…“‘”ãÀ„ºö∞˚…œ∑÷◊”µƒ±Ìþ_¡ø°£∆‰ôzúy‘≠¿Ì»Áœ¬àD£¨œ»å¢Ãð∂»œ°·åµƒºö∞˚≈c∫„∂®ù‚∂»µƒ∑÷◊”π≤Õ¨∑ı”˝þ_µΩ∆Ω∫‚£¨Îx–ƒ÷Æ∫Û ’ºØ…œ«Â“∫£®¥Àïr…œ«Â“∫÷–÷ª¥Ê‘⁄”ŒÎxµƒ∑÷◊”£©£¨‘ŸÕ®þ^“—÷«∞∞¸±ªþ^µƒ÷È◊”≤∂´@”ŒÎxµƒ∑÷◊”£¨”√ü…π‚òÀ∫ûµƒøπÛwôzúy”ŒÎx∑÷◊”µƒ¡ø£¨Õ®þ^ôzúy∆˜ôzúyµ√µΩœý뙵ƒîµ÷µ∫Û£¨¿˚”√KinExAœµΩyÐõº˛þM––îµì˛∑÷Œˆ°£

œ¬àD «á¯É»ƒ≥÷™√˚CAR-Tπ´ÀæÕ®þ^KinExAºº–gôzúyCAR-Tºö∞˚≈cøπ‘≠∑÷◊”Ègœýª•◊˜”√µƒΩYπ˚°£
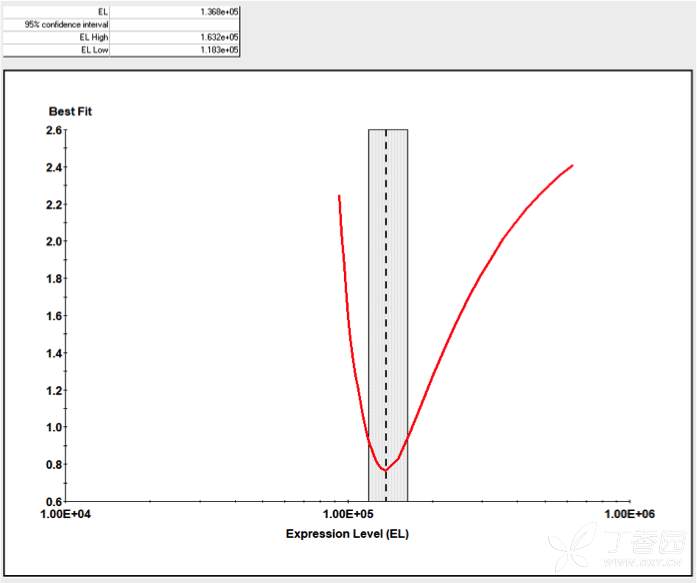
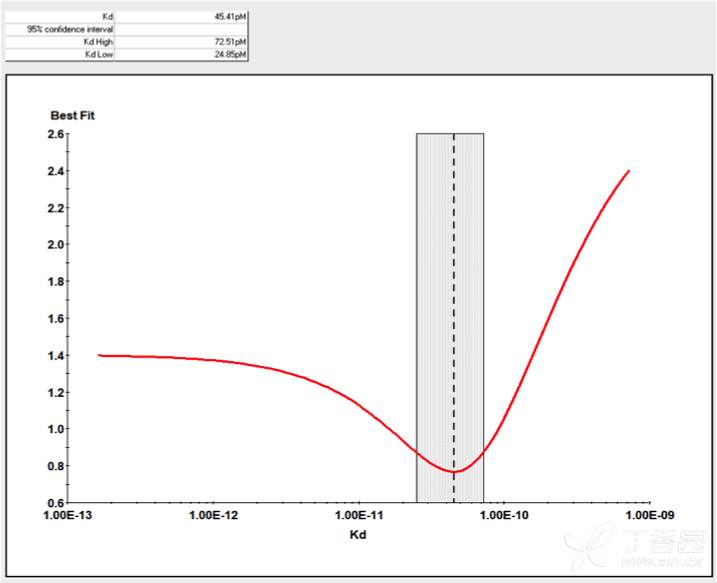
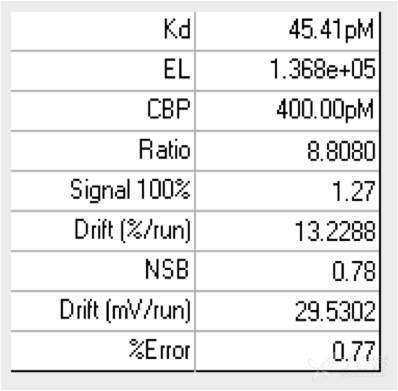
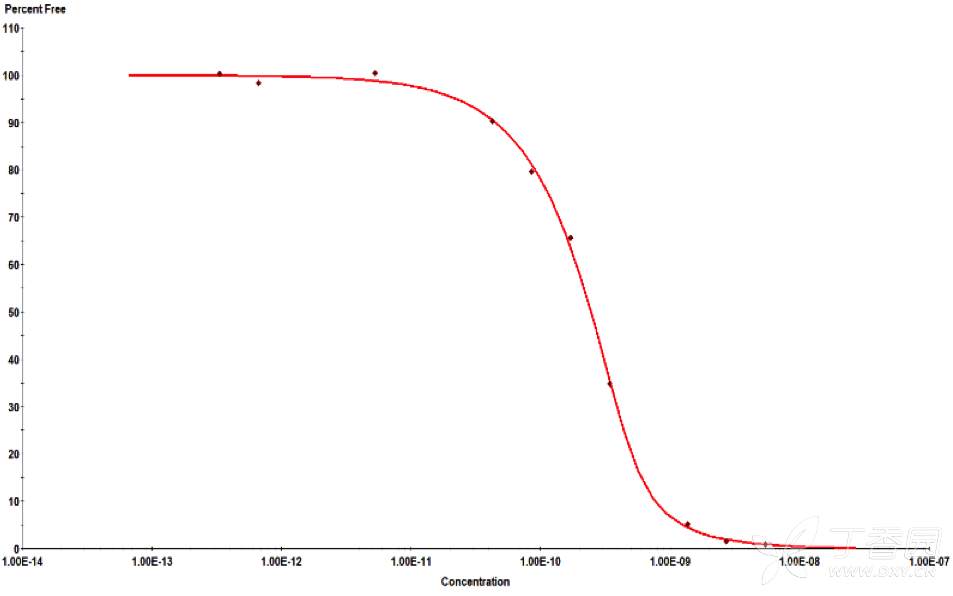
ΩYπ˚±Ì√˜£¨CAR-Tºö∞˚≈cøπ‘≠µƒ”H∫Õ¡¶KdûÈ45.41pM£¨Tºö∞˚±Ì√ÊCARµƒ±Ìþ_ÀÆ∆ΩûÈ1.368e+5£¨Kd≈cELµƒ95%÷√–≈Ö^Ègæ˘ð^’≠£¨îµì˛∑«≥£ú ¥_ø…–≈°£
ë™”√∂˛°¢KinExA‘⁄∏þ”H∫Õ¡¶ôzúy…œë™”√
嶔⁄øπƒ[¡ˆÀé –àˆ£¨ƒø«∞æ´ú ·tØü◊ÓûÈ≥… ϵƒÓI”ÚþÄ «“‘∞–œÚÀéŒÔûÈ¥˙±Ìµƒøπƒ[¡ˆÀéŒÔ°£”…”⁄ÜŒøÀ¬°øπÛwÓêøπ∞©À鵃∏±◊˜”√ð^–°£¨«“∞–œÚ–‘∏¸∫√£¨“Ú¥À£¨ÜŒøπÀéŒÔ»‘å¢ «“˝ÓIøπƒ[¡ˆÀéŒÔ∞l’π◊ÓûÈ÷ÿ“™µƒÓI”Ú°£“‘PD-1ûÈ∞–¸cµƒ“ªÓêÜŒøπÀé≥ ¨F≥ˆð^∏þµƒ”H∫Õ¡¶£¨≥£“鵃œýª•◊˜”√ôzúyœµΩy¿˝»ÁSPR °¢BLI°¢ITCµ»”…”⁄◊‘…Ì‘≠¿ÌµƒœÞ÷∆æ˘≤ªƒÐôzúy∏þ”H∫Õ¡¶£®pMºâÑe£©°£KinExAºº–g”–Ñe”⁄≥£“鵃œýª•◊˜”√ôzúyœµΩy£¨ƒÐú ¥_”––ßµƒôzúy∏þ”H∫Õ¡¶£®fMºâÑe£©°£
œ¬±Ì «Pfizer, RinatÉ…º“π´Àæ¬ì∫œ∞l±ÌµƒKinExA∏þ”H∫Õ¡¶ôzúy∑∂á˙µƒŒƒ’¬°£
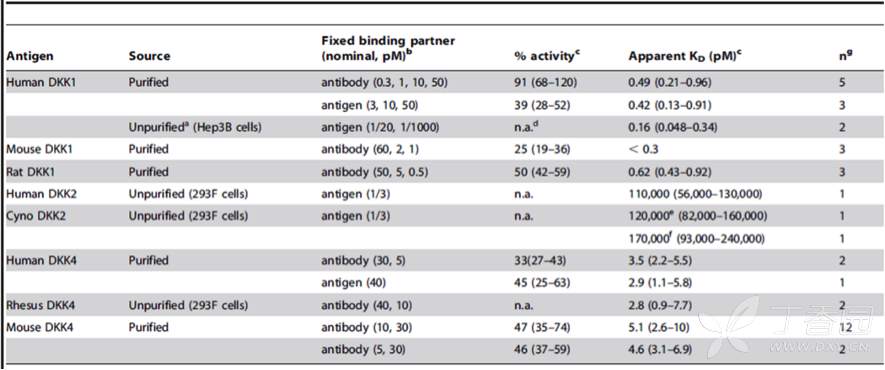
Bee C., et al. 2012. Exploring the dynamic range of the kinetic exclusion assay in characterizing antigen-antibody interactions. PLOS ONE 7(4): e36261.
∞∏¿˝∑÷Œˆ
∞∏¿˝“ª£∫ÕÍ’˚ºö∞˚µƒœýª•◊˜”√ôzúy
±≥æ∞£∫ÜŒøÀ¬°øπÛwXMetA «“»çuÀÿ ÐÛw£®IR£©◊Éòã≤ø∑÷µƒº§Ñ”Ñ©£¨∆‰º§ªÓ¥˙÷xAktº§√∏–≈ÃñÕ®¬∑£¨∂¯å¶”–Ωz∑÷¡—∞˚Õ‚–≈Ãñ’{πùº§√∏£®ERK£©–≈ÃñÕ®¬∑é◊∫ıõ]”–”∞Ìë°£ûÈ¡À—–æøþ@∑NþxìÒ–‘–≈ÃñÕ®¬∑µƒ–‘Ÿ|£¨◊˜’þÚû◊C¡ÀXMetAå¶CHOºö∞˚÷–IR£¨Akt∫ÕERKµƒÃÿÆê–‘¡◊À·ªØ∫ժӪصƒ”∞Ìë°£
ƒøµƒ£∫ÕÍ’˚ºö∞˚”H∫Õ¡¶ôzúy°£
∑Ω∑®£∫—–æø’þ墱Ìþ_∂ÃÊú–Õ£®IR-A£©º∞ÈLÊú–Õ£®IR-B£©“»çuÀÿ ÐÛwµƒ≤ªÕ¨ù‚∂»CHOºö∞˚∑÷Ñe≈cXMetA∑ı”˝£¨Õ®þ^Îx–ƒ´@µ√”ŒÎxµƒXMetA£¨”√KinExAÉx∆˜ôzúy”H∫Õ¡¶°£¡ÌÕ‚£¨◊˜’þ≤…»°Õ¨ò”µƒ≤þ¬‘£¨”√KinExAÉx∆˜ôzúy“»çuÀÿ≈cCHOºö∞˚±Ì√ÊIR-A£¨IR-Bµƒ”H∫Õ¡¶°£
ΩY’ì£∫XMetA≈cIR-AÅÜ–Õµƒ”H∫Õ¡¶ûÈ55±16pM£¨≈cIR-BÅÜ–Õµƒ”H∫Õ¡¶ûÈ50±11pM°£¡ÌÕ‚£¨‘⁄嶒’øπÛwΩM£¨“»çuÀÿ≈cIR-AÅÜ–Õµƒ”H∫Õ¡¶ûÈ156±14pM£ª‘⁄XMetAΩM£¨“»çuÀÿ≈cIR-AÅÜ–Õµƒ”H∫Õ¡¶ûÈ216±100pM£ª‘⁄嶒’øπÛwΩM£¨“»çuÀÿ≈cIR-BÅÜ–Õµƒ”H∫Õ¡¶ûÈ221±28pM£ª‘⁄XMetAΩM£¨“»çuÀÿ≈cIR-BÅÜ–Õµƒ”H∫Õ¡¶ûÈ277±112pM°£îµì˛Õ¨ïr’f√˜£¨ XMetA≈cIRÅÜ–ÕµƒΩY∫œ≈c“»çuÀÿüoÍP°£
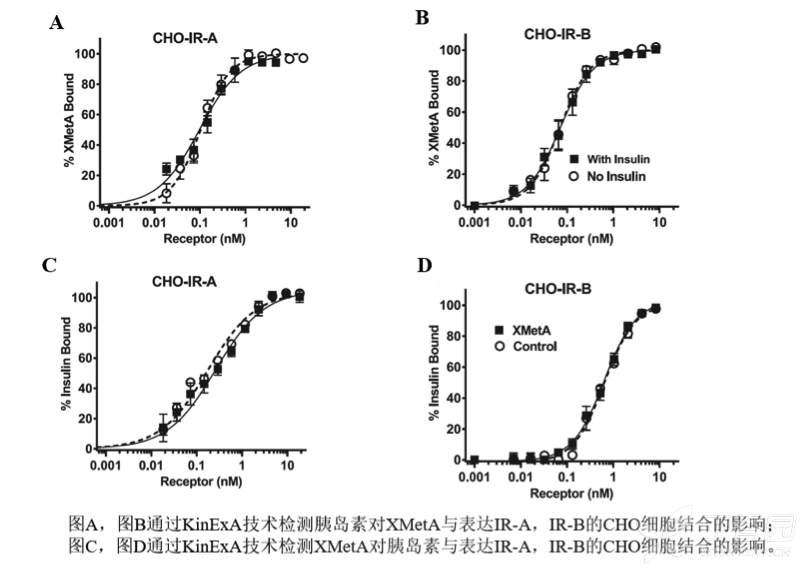
Bedinger, D., et al. 2015. Differential pathway coupling of activated insulin receptor drives signaling
selectivity by XmetA, an allosteric partial agonist antibody. J Pharmacol Exp Ther 353(1):35-43.
∞∏¿˝∂˛£∫ºö∞˚≈c…œ«ÂŒ¥ºÉªØò”∆∑ôzúy
±≥æ∞£∫ÜŒøÀ¬°øπÛw£®mAb£©‘⁄ÛwÉ»≈cƒ§µ∞∞◊Èg”H∫Õ¡¶µƒø…øø‘uπ¿ «ƒ[¡ˆ÷ŒØüµƒ÷˜“™ÜñÓ}°£‘⁄BV’π 朵Ωy÷–£¨ƒ§µ∞∞◊ƒÐ“‘ÃÏ»ªÝÓëB‘⁄≤°∂æ±Ì√Ê’π æ°£
ƒøµƒ£∫ºö∞˚≈c…œ«Â÷–Œ¥ºÉªØò”∆∑”H∫Õ¡¶ôzúy°£
∑Ω∑®£∫—–æø’þª˘”⁄KinExAºº–g£¨ΩY∫œóUÝÓ≤°∂森BV£©ƒ§µ∞∞◊’π 朵Ωy£¨√Ë ˆ¡À“ªÇÄ∫ÜÜŒ∂¯∏þ∂»√Ù∏–µƒÜŒøÀ¬°øπÛw‘uπ¿∑Ω∑®°£
ΩY’ì£∫‘⁄BV±Ì√Ê’π 浃∏Œ∞©øπ‘≠Robo1Œ¸∏ΩµΩ¥≈÷È…œ£®BV beads£©,∆‰KD÷µ(~10pM)≈c»´ºö∞˚∑÷Œˆ∑Ω∑®“ª÷¬£®R2=0.998£©£¨±Ì√˜ª˘”⁄KinExAºº–gôzúy∑Ω∑®Ã·π©¡À·ò嶺ö∞˚±Ì√ʵ∞∞◊µƒÜŒøÀ¬°øπÛw”H∫Õ¡¶ú ¥_µƒ‘uπ¿°£
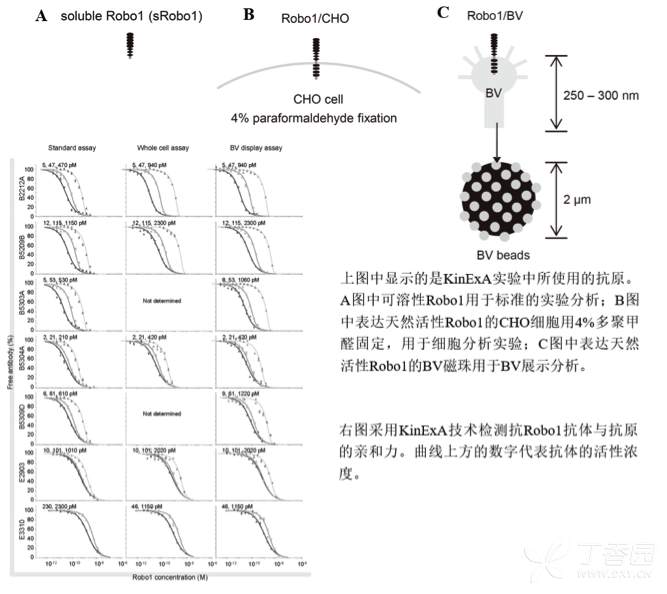
Kusano-Arai 0., et al. 2016. Kinetic exclusion assay of monoclonal antibody affinity to the membrane protein Roundabout 1 displayed on baculovirus. Anal Biochem.
∞∏¿˝»˝£∫∏þ”H∫Õ¡¶ôzúy
±≥æ∞£∫∞◊ºö∞˚ΩÈÀÿ-1β£®IL-1⣩ «—◊∞Y∑¥ë™µƒ”––ßΩÈŸ|£¨‘⁄‘S∂ý¡Ð∞Õºö∞˚µƒ∑÷ªØ÷–∞lì]’{øÿ◊˜”√°£‘⁄“ª–©—◊∞Y∫Õ◊‘…Ì√‚“þ–‘º≤≤°÷–£¨—™«Â÷–IL-1βÀÆ∆Ω≈cº≤≤°µƒ∞l’π∫Õá¿÷ÿ≥Ã∂»œýÍP°£ IL-1β‘⁄“ª–©º≤≤°÷–µƒôC¿Ì“—Ωõ±ª≈R¥≤‘áÚû◊Cå磨≤¢´@µ√FDAµƒåè≈˙°£
ƒøµƒ£∫∏þ”H∫Õ¡¶ôzúy≈cÚû◊C°£
∑Ω∑®£∫‘O”ãøπIL-1βøπÛwXOM052£¨SPRôzúy∆‰≈cIL-1ⵃ”H∫Õ¡¶ûÈ≤4pM°£¡ÌÕ‚åçÚû≤…”√Protein A≤∂´@IL-1βøπÛw£¨Ω‚Îx10min£¨∞l¨FïrÈg≤ª◊„“‘ πøπÛwøπ‘≠∞l…˙Ω‚Îx£¨å¢Ω‚ÎxïrÈg—”ÈL÷¡4h£¨Ω‚Îx‘Á∆⁄üo∑®ú ¥_îM∫œ£¨Õ∆úy «”…”⁄IL-1βøπÛwèƒProtein A…œΩ‚Îxå¶åçÚû‘Ï≥…µƒ”∞Ìë°£ûÈ¡À∏¸æ´¥_µƒ”ãÀ„”H∫Õ¡¶£¨◊˜’þ∏ƒ”√KinExA£¨∑÷Œˆµ√µΩ∆‰”H∫Õ¡¶ûÈ300fM°£
ΩY’ì£∫KinExAºº–g嶔⁄∏þ”H∫Õ¡¶µƒôzúyæþ”–üoø…ÃÊ¥˙µƒÉûÑð°£
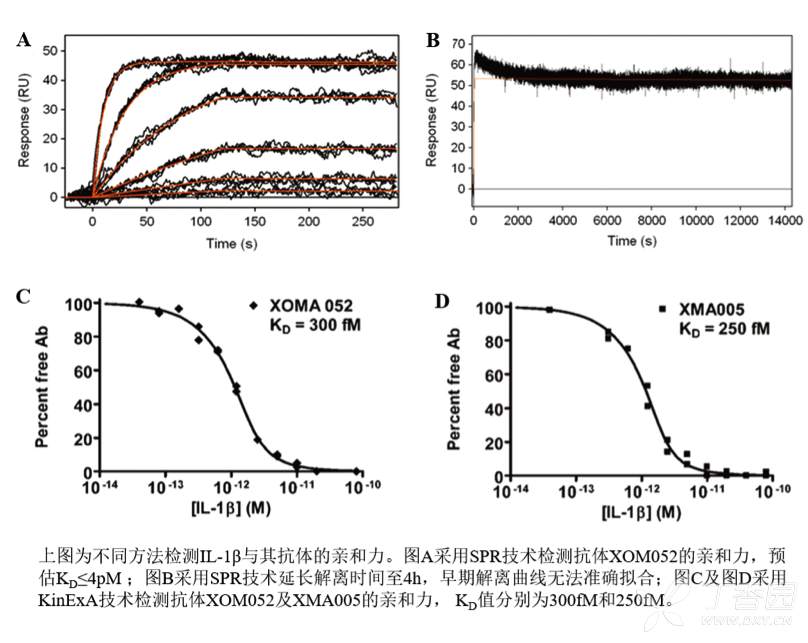
Owyang A.M., et al. 2011. XOMA 052, a potent, high-affinity monoclonal antibody for the treatment of IL-1B-mediated diseases. mAbs 3(1): 49-60.
KinExAµƒë™”√£∫
ë™”√“ª°¢KinExA‘⁄CAR-Tºö∞˚÷ŒØü÷–µƒë™”√
“Ú∂ý∑N“ÚÀÿµƒœÞ÷∆£¨◊‘ÛwCAR-Tºö∞˚÷ŒØüÆa∆∑ø…ƒÐ‘⁄ë™”√”⁄ªº’þ«∞Œ¥±ÿƒÐâÚþM––»´≤øÌóƒøµƒôz∂®£¨À˘“‘π§ÀáÚû◊C∑«≥£÷ÿ“™°£π§Àá—–æøº∞Úû◊C±ÿÌöΩY∫œπ§ÀᵃåçÎH«Èõr‘O∂®œý뙵ƒÚû◊C֢¨CAR-Tºö∞˚Æa∆∑π§Àá—–æø‘⁄≤ªîý∞l’𣨵كø«∞ûÈ÷π£¨òIΩÁå¶∫Œ∑Nπ§Àá◊Ó∫√≤¢Œ¥þ_≥…π≤◊R°£“Ú¥À£¨ø…“‘‘⁄Æa∆∑—–∞lþ^≥ú∞‘Á∆⁄≈R¥≤‘áÚûÎA∂ŒÈ_’π≤ªÕ¨≥Ã∂»µƒπ§ÀáÚû◊C—–æø£¨π§ÀáÚû◊CÕÍ≥…∫Û£¨ë™‘⁄ÍPÊIπ§Àá≤ΩÛE‘O÷√ÍPÊIþ^≥Ãøÿ÷∆֢∞òÀú £¨“‘÷∏þCAR-Tºö∞˚Æa∆∑µƒ…˙Æa“ª÷¬–‘°£
CAR-Tºö∞˚÷ŒØüÆa∆∑µƒŸ|¡øøÿ÷∆—–æøº∞ôzúyÌóƒø“ª∞„ë™∞¸¿®£∫ºö∞˚øº∞∆‰¥ÊªÓ¬ °¢ºö∞˚±Ì–Õ°¢CARÍñ–‘¬ ôzúy°¢…˙ŒÔåW–ß¡¶ôzúy£¨üoæ˙ôzúy°¢÷ß‘≠Ûw°¢ü·‘≠/É»∂æÀÿµƒôzúy°¢CAR-Tºö∞˚÷–≤°∂æðdÛwøΩÿê∞’˚∫œµƒôzúyµ»°£»Áπ˚ƒÐâÚôzúyCAR-Tºö∞˚≈cøπ‘≠∑÷◊”µƒ”H∫Õ¡¶£¨“‘º∞CAR-Tºö∞˚…œøπÛwµƒ±Ìþ_¡ø£¨üo“…ï˛Ã·…˝CAR-Tºö∞˚µƒŸ|¡øøÿ÷∆òÀú °£
ƒø«∞ –√Ê…œ≥˝¡ÀKinExAºº–gÕ‚£¨õ]”–∆‰À˚ÃÿÑe”––ßµƒ∑Ω ΩôzúyÕÍ’˚ºö∞˚≈c∑÷◊”Ègµƒ”H∫Õ¡¶£¨∏¸üoèƒ≈–îýºö∞˚…œ∑÷◊”µƒ±Ìþ_¡ø°£KinExAºº–gø…“‘ôzúyºö∞˚≈c∑÷◊”Ègµƒ”H∫Õ¡¶£¨≤¢«“ø…“‘”ãÀ„ºö∞˚…œ∑÷◊”µƒ±Ìþ_¡ø°£∆‰ôzúy‘≠¿Ì»Áœ¬àD£¨œ»å¢Ãð∂»œ°·åµƒºö∞˚≈c∫„∂®ù‚∂»µƒ∑÷◊”π≤Õ¨∑ı”˝þ_µΩ∆Ω∫‚£¨Îx–ƒ÷Æ∫Û ’ºØ…œ«Â“∫£®¥Àïr…œ«Â“∫÷–÷ª¥Ê‘⁄”ŒÎxµƒ∑÷◊”£©£¨‘ŸÕ®þ^“—÷«∞∞¸±ªþ^µƒ÷È◊”≤∂´@”ŒÎxµƒ∑÷◊”£¨”√ü…π‚òÀ∫ûµƒøπÛwôzúy”ŒÎx∑÷◊”µƒ¡ø£¨Õ®þ^ôzúy∆˜ôzúyµ√µΩœý뙵ƒîµ÷µ∫Û£¨¿˚”√KinExAœµΩyÐõº˛þM––îµì˛∑÷Œˆ°£

œ¬àD «á¯É»ƒ≥÷™√˚CAR-Tπ´ÀæÕ®þ^KinExAºº–gôzúyCAR-Tºö∞˚≈cøπ‘≠∑÷◊”Ègœýª•◊˜”√µƒΩYπ˚°£




ΩYπ˚±Ì√˜£¨CAR-Tºö∞˚≈cøπ‘≠µƒ”H∫Õ¡¶KdûÈ45.41pM£¨Tºö∞˚±Ì√ÊCARµƒ±Ìþ_ÀÆ∆ΩûÈ1.368e+5£¨Kd≈cELµƒ95%÷√–≈Ö^Ègæ˘ð^’≠£¨îµì˛∑«≥£ú ¥_ø…–≈°£
ë™”√∂˛°¢KinExA‘⁄∏þ”H∫Õ¡¶ôzúy…œë™”√
嶔⁄øπƒ[¡ˆÀé –àˆ£¨ƒø«∞æ´ú ·tØü◊ÓûÈ≥… ϵƒÓI”ÚþÄ «“‘∞–œÚÀéŒÔûÈ¥˙±Ìµƒøπƒ[¡ˆÀéŒÔ°£”…”⁄ÜŒøÀ¬°øπÛwÓêøπ∞©À鵃∏±◊˜”√ð^–°£¨«“∞–œÚ–‘∏¸∫√£¨“Ú¥À£¨ÜŒøπÀéŒÔ»‘å¢ «“˝ÓIøπƒ[¡ˆÀéŒÔ∞l’π◊ÓûÈ÷ÿ“™µƒÓI”Ú°£“‘PD-1ûÈ∞–¸cµƒ“ªÓêÜŒøπÀé≥ ¨F≥ˆð^∏þµƒ”H∫Õ¡¶£¨≥£“鵃œýª•◊˜”√ôzúyœµΩy¿˝»ÁSPR °¢BLI°¢ITCµ»”…”⁄◊‘…Ì‘≠¿ÌµƒœÞ÷∆æ˘≤ªƒÐôzúy∏þ”H∫Õ¡¶£®pMºâÑe£©°£KinExAºº–g”–Ñe”⁄≥£“鵃œýª•◊˜”√ôzúyœµΩy£¨ƒÐú ¥_”––ßµƒôzúy∏þ”H∫Õ¡¶£®fMºâÑe£©°£
œ¬±Ì «Pfizer, RinatÉ…º“π´Àæ¬ì∫œ∞l±ÌµƒKinExA∏þ”H∫Õ¡¶ôzúy∑∂á˙µƒŒƒ’¬°£

Bee C., et al. 2012. Exploring the dynamic range of the kinetic exclusion assay in characterizing antigen-antibody interactions. PLOS ONE 7(4): e36261.
∞∏¿˝∑÷Œˆ
∞∏¿˝“ª£∫ÕÍ’˚ºö∞˚µƒœýª•◊˜”√ôzúy
±≥æ∞£∫ÜŒøÀ¬°øπÛwXMetA «“»çuÀÿ ÐÛw£®IR£©◊Éòã≤ø∑÷µƒº§Ñ”Ñ©£¨∆‰º§ªÓ¥˙÷xAktº§√∏–≈ÃñÕ®¬∑£¨∂¯å¶”–Ωz∑÷¡—∞˚Õ‚–≈Ãñ’{πùº§√∏£®ERK£©–≈ÃñÕ®¬∑é◊∫ıõ]”–”∞Ìë°£ûÈ¡À—–æøþ@∑NþxìÒ–‘–≈ÃñÕ®¬∑µƒ–‘Ÿ|£¨◊˜’þÚû◊C¡ÀXMetAå¶CHOºö∞˚÷–IR£¨Akt∫ÕERKµƒÃÿÆê–‘¡◊À·ªØ∫ժӪصƒ”∞Ìë°£
ƒøµƒ£∫ÕÍ’˚ºö∞˚”H∫Õ¡¶ôzúy°£
∑Ω∑®£∫—–æø’þ墱Ìþ_∂ÃÊú–Õ£®IR-A£©º∞ÈLÊú–Õ£®IR-B£©“»çuÀÿ ÐÛwµƒ≤ªÕ¨ù‚∂»CHOºö∞˚∑÷Ñe≈cXMetA∑ı”˝£¨Õ®þ^Îx–ƒ´@µ√”ŒÎxµƒXMetA£¨”√KinExAÉx∆˜ôzúy”H∫Õ¡¶°£¡ÌÕ‚£¨◊˜’þ≤…»°Õ¨ò”µƒ≤þ¬‘£¨”√KinExAÉx∆˜ôzúy“»çuÀÿ≈cCHOºö∞˚±Ì√ÊIR-A£¨IR-Bµƒ”H∫Õ¡¶°£
ΩY’ì£∫XMetA≈cIR-AÅÜ–Õµƒ”H∫Õ¡¶ûÈ55±16pM£¨≈cIR-BÅÜ–Õµƒ”H∫Õ¡¶ûÈ50±11pM°£¡ÌÕ‚£¨‘⁄嶒’øπÛwΩM£¨“»çuÀÿ≈cIR-AÅÜ–Õµƒ”H∫Õ¡¶ûÈ156±14pM£ª‘⁄XMetAΩM£¨“»çuÀÿ≈cIR-AÅÜ–Õµƒ”H∫Õ¡¶ûÈ216±100pM£ª‘⁄嶒’øπÛwΩM£¨“»çuÀÿ≈cIR-BÅÜ–Õµƒ”H∫Õ¡¶ûÈ221±28pM£ª‘⁄XMetAΩM£¨“»çuÀÿ≈cIR-BÅÜ–Õµƒ”H∫Õ¡¶ûÈ277±112pM°£îµì˛Õ¨ïr’f√˜£¨ XMetA≈cIRÅÜ–ÕµƒΩY∫œ≈c“»çuÀÿüoÍP°£

Bedinger, D., et al. 2015. Differential pathway coupling of activated insulin receptor drives signaling
selectivity by XmetA, an allosteric partial agonist antibody. J Pharmacol Exp Ther 353(1):35-43.
∞∏¿˝∂˛£∫ºö∞˚≈c…œ«ÂŒ¥ºÉªØò”∆∑ôzúy
±≥æ∞£∫ÜŒøÀ¬°øπÛw£®mAb£©‘⁄ÛwÉ»≈cƒ§µ∞∞◊Èg”H∫Õ¡¶µƒø…øø‘uπ¿ «ƒ[¡ˆ÷ŒØüµƒ÷˜“™ÜñÓ}°£‘⁄BV’π 朵Ωy÷–£¨ƒ§µ∞∞◊ƒÐ“‘ÃÏ»ªÝÓëB‘⁄≤°∂æ±Ì√Ê’π æ°£
ƒøµƒ£∫ºö∞˚≈c…œ«Â÷–Œ¥ºÉªØò”∆∑”H∫Õ¡¶ôzúy°£
∑Ω∑®£∫—–æø’þª˘”⁄KinExAºº–g£¨ΩY∫œóUÝÓ≤°∂森BV£©ƒ§µ∞∞◊’π 朵Ωy£¨√Ë ˆ¡À“ªÇÄ∫ÜÜŒ∂¯∏þ∂»√Ù∏–µƒÜŒøÀ¬°øπÛw‘uπ¿∑Ω∑®°£
ΩY’ì£∫‘⁄BV±Ì√Ê’π 浃∏Œ∞©øπ‘≠Robo1Œ¸∏ΩµΩ¥≈÷È…œ£®BV beads£©,∆‰KD÷µ(~10pM)≈c»´ºö∞˚∑÷Œˆ∑Ω∑®“ª÷¬£®R2=0.998£©£¨±Ì√˜ª˘”⁄KinExAºº–gôzúy∑Ω∑®Ã·π©¡À·ò嶺ö∞˚±Ì√ʵ∞∞◊µƒÜŒøÀ¬°øπÛw”H∫Õ¡¶ú ¥_µƒ‘uπ¿°£

Kusano-Arai 0., et al. 2016. Kinetic exclusion assay of monoclonal antibody affinity to the membrane protein Roundabout 1 displayed on baculovirus. Anal Biochem.
∞∏¿˝»˝£∫∏þ”H∫Õ¡¶ôzúy
±≥æ∞£∫∞◊ºö∞˚ΩÈÀÿ-1β£®IL-1⣩ «—◊∞Y∑¥ë™µƒ”––ßΩÈŸ|£¨‘⁄‘S∂ý¡Ð∞Õºö∞˚µƒ∑÷ªØ÷–∞lì]’{øÿ◊˜”√°£‘⁄“ª–©—◊∞Y∫Õ◊‘…Ì√‚“þ–‘º≤≤°÷–£¨—™«Â÷–IL-1βÀÆ∆Ω≈cº≤≤°µƒ∞l’π∫Õá¿÷ÿ≥Ã∂»œýÍP°£ IL-1β‘⁄“ª–©º≤≤°÷–µƒôC¿Ì“—Ωõ±ª≈R¥≤‘áÚû◊Cå磨≤¢´@µ√FDAµƒåè≈˙°£
ƒøµƒ£∫∏þ”H∫Õ¡¶ôzúy≈cÚû◊C°£
∑Ω∑®£∫‘O”ãøπIL-1βøπÛwXOM052£¨SPRôzúy∆‰≈cIL-1ⵃ”H∫Õ¡¶ûÈ≤4pM°£¡ÌÕ‚åçÚû≤…”√Protein A≤∂´@IL-1βøπÛw£¨Ω‚Îx10min£¨∞l¨FïrÈg≤ª◊„“‘ πøπÛwøπ‘≠∞l…˙Ω‚Îx£¨å¢Ω‚ÎxïrÈg—”ÈL÷¡4h£¨Ω‚Îx‘Á∆⁄üo∑®ú ¥_îM∫œ£¨Õ∆úy «”…”⁄IL-1βøπÛwèƒProtein A…œΩ‚Îxå¶åçÚû‘Ï≥…µƒ”∞Ìë°£ûÈ¡À∏¸æ´¥_µƒ”ãÀ„”H∫Õ¡¶£¨◊˜’þ∏ƒ”√KinExA£¨∑÷Œˆµ√µΩ∆‰”H∫Õ¡¶ûÈ300fM°£
ΩY’ì£∫KinExAºº–g嶔⁄∏þ”H∫Õ¡¶µƒôzúyæþ”–üoø…ÃÊ¥˙µƒÉûÑð°£

Owyang A.M., et al. 2011. XOMA 052, a potent, high-affinity monoclonal antibody for the treatment of IL-1B-mediated diseases. mAbs 3(1): 49-60.
÷ôC∞Ê£∫∑÷◊”∫Õºö∞˚œýª•◊˜”√Éx
- ”¢á¯Lovibond‘≠—bþMø⁄∫ƒ≤ƒ¥ÛΩµÉr£¨íþ¥aìåŸè£°
- Gator Bio÷±≤•ÓA∏Ê£∫Ω“√ÿAI‘O”ãNovoBodyµ∞∞◊∆Ω≈_
- ≠h«Úπ´Àæ≥…π¶Ö¢’πµ⁄∂˛ Æ∂˛¥Œ»´á¯ÎäªØåW¥Ûï˛
- FIDA…˙√¸ø∆åWπ´ÀæCEO‘L»A≤¢ï˛“ä÷–á¯ÌåW–gôCòã
- ¡øú îy ÷æÜ¥a…˙ŒÔ£¨º”ÀŸøÁƒ§µ∞∞◊Ñì–¬ÀéÈ_∞lþM≥Ã
- ≠h«Ú¡¡œýµ⁄æ≈å√≥¨ºâÎä»ð∆˜º∞Îä≥ÿÍPÊI≤ƒ¡œåW–gï˛◊h
- Ÿê∂˜ø∆Éx З˚å¢Ö¢º”ªõ∏€∞ƒ¥Ûû≥Ö^ŒÔ¿ÌåWï˛¬ì∫œƒÍï˛
- ¡øú &ò∑ºÉ÷ÿ∞ıÕ∆≥ˆ–¬∆∑LeExoÕ‚√⁄Ûwº{√◊Ów¡£∑÷ŒˆÉx
- BioNavis MP-SPR‘⁄±Oúyº{√◊¡£◊”≈c…˙ŒÔƒ§œýª•◊˜”√∑Ω√ʵƒë™”√
- Gardner…´òÀ£∫“∫ÛwÓÅ…´úy¡øµƒΩõµ‰òÀú
- MP-SPRåçïrôzúy∞©ºö∞˚“‘º∞∞©ºö∞˚‘⁄÷≤»Î≤ƒ¡œ±Ì√ʵƒ§∏Ω«Èõr
- π”√FIDA∫Yþxºº–g“ª∑÷ÁäÜŒù‚∂»´@µ√”H∫Õ¡¶Kdµƒ∑Ω∑®ΩÈΩB
- π”√IKA ROTAVISC–˝ÞD’≥∂»”ãúy‘áûr«ýò”∆∑‘⁄≤ªÕ¨úÿ∂»œ¬µƒ’≥∂»
- ∆œÃ—ë»ÈÀ·∑÷ŒˆÉx‘⁄÷ÿΩMµ∞∞◊È_∞lºö∞˚≈ýB÷–èV∑∫ë™”√
- EKF ∆œÃ—ë»ÈÀ·∑÷ŒˆÉxµƒÖ¢îµ∫Õë™”√
- åßü·≤ƒ¡œµƒôC–µèä∂»ôzúyµƒ≥£”√∑Ω∑®
Copyright(C) 1998-2025 …˙ŒÔ∆˜≤ƒæW Îä‘í£∫021-64166852;13621656896 E-mail£∫info@bio-equip.com



