無細胞表達系統——難度蛋白表達的福音
1964年有兩個人開創了體外蛋白表達的先河,這兩個人的名字大家必定不會陌生—馬太和尼倫伯格。因為他們的創新思維讓人類破譯了編碼氨基酸的64種翻譯密碼子。從此,體外蛋白表達開始為科學界所關注,不過彼時這個系統蛋白表達量低、持續時間短、穩定性差,使其未能得到進一步發展。
到80年代中期Spirin等對其進行優化提高了蛋白合成產率之后,體外蛋白表達系統—無細胞表達系統,開始為生物工程領域所逐步重視,逐步發展出多種類型的無細胞表達體系。常用的有四種:大腸桿菌抽提物無細胞表達系統、酵母抽提物無細胞表達系統、小麥胚芽抽提物無細胞表達系統和兔網織紅細胞抽提物無細胞表達系統。
利用細胞抽提物(比如大腸桿菌、酵母細胞、小麥胚芽、兔紅血球細胞等)提供RNA聚合酶、tRNA、核糖體、氨基酸、起始因子、延伸因子、終止因子等物質,添加表達模板質粒或PCR產物,并不斷提供反應底物氨基酸、能量-ATP等物質,同時通過透析等手段去除反應副產物,在體外環境中進行蛋白的表達,這項技術稱為無細胞表達技術。
無細胞表達的幾大重磅級優勢:
1. 無細胞表達系統最大優勢是避開了細胞內環境對細胞表達的影響,可以人為控制反應條件和進程。金開瑞生物的無細胞表達系統可對系統進行各項優化,如Tag優化、M優化、K優化,以此得到最優表達條件。
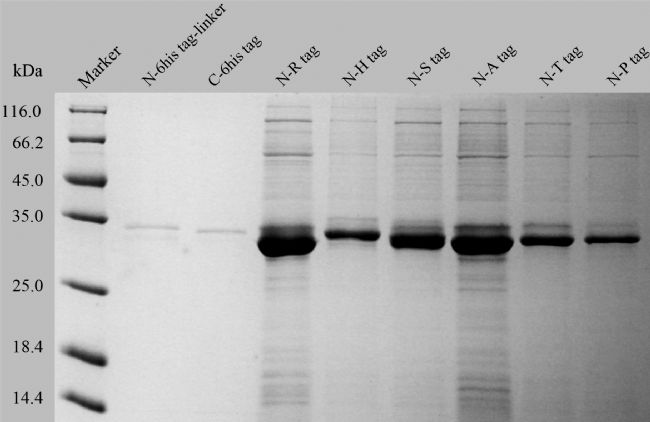
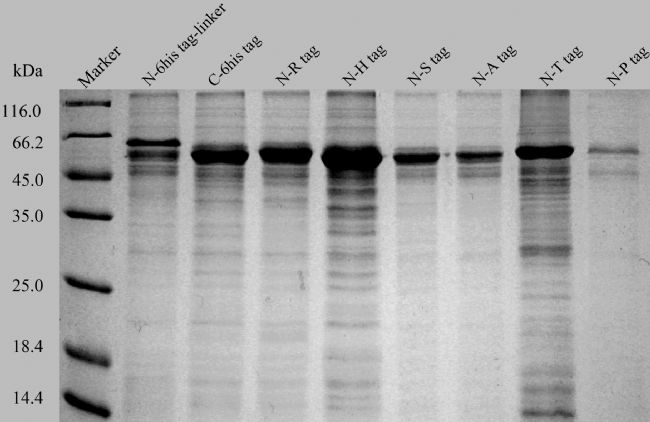
對yua3蛋白的Tag優化
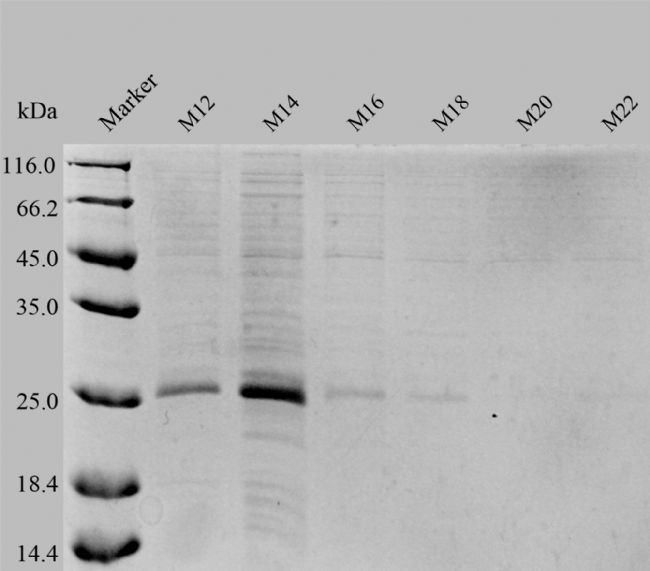
對VACV I5蛋白的M優化
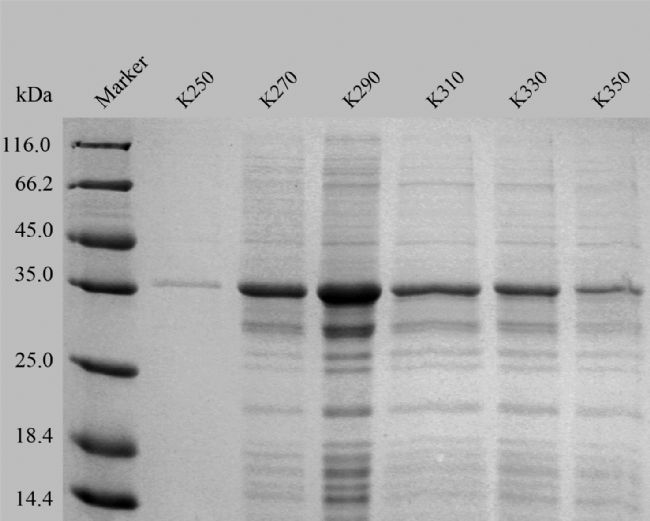
對TMEM65蛋白的K優化
2. 大大縮短實驗周期。普通的表達過程需要2~3天,無細胞的表達過程則大大縮短到1~2小時,節省了不少時間成本,為那些著急畢業的實驗小伙伴解決了燃眉之急。
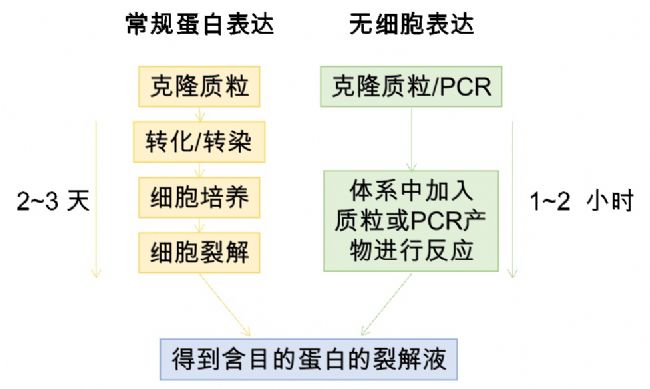
3. 對常規細胞內表達難以表達的蛋白也可輕松解決,例如膜蛋白和毒性蛋白等。哺乳動物基因組的近三分之一由膜蛋白組成,其中約一半可以成為藥物靶標,研究這些靶標膜蛋白,開發潛在的生物靶向藥物,對疾病的致病機理及藥物開發具有重要意義。

七次跨膜蛋白ADRB2的表達
毒性蛋白ExoU的表達
4.可以制備蛋白復合物,研究蛋白的相互作用。無細胞系統表達的蛋白可用于下游pull-down及凝膠遷移試驗,研究蛋白-蛋白及蛋白-核酸相互作用。
5.可在特定位點插入非天然氨基酸。在特定位點插入非天然氨基酸,對重組蛋白類藥物的研發具有重大意義。
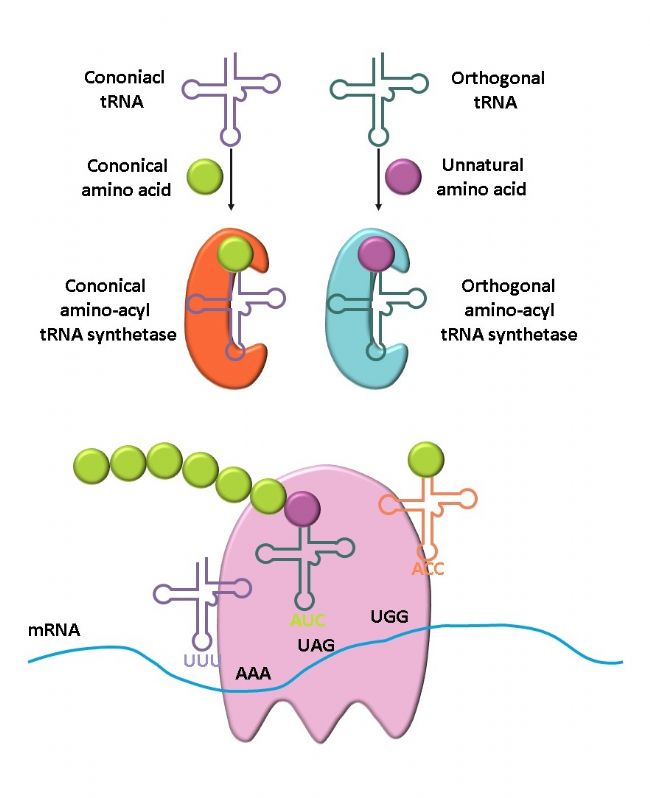
非天然氨基酸引入原理
6.可用于表達類顆粒病毒。這個表達產物既具有引起免疫響應的能力,又不含遺傳物質。所以無法復制,是一類理想的病毒類疫苗。
如何選擇合適的蛋白表達系統呢?請點擊這里!