重組蛋白在靶點藥物開發領域的應用
具有藥理活性的生物 “靶點” 一般指藥物直接結合的那些蛋白質,比如酶、離子通道和受體或其他生物分子 (如 DNA、RNA、肝素和肽)。大多數藥物靶點是蛋白質,用于治療或診斷疾病的化學物質與靶標蛋白發生選擇性相互作用,致使其生物途徑或功能改變。
大多數藥物靶點屬于五個蛋白質家族:G 蛋白偶聯受體 (GPCR)、離子通道、激酶、核激素受體和蛋白酶。G 蛋白偶聯受體和酶是美國食品及藥物管理局 (FDA) 獲批藥物兩大類靶標蛋白。
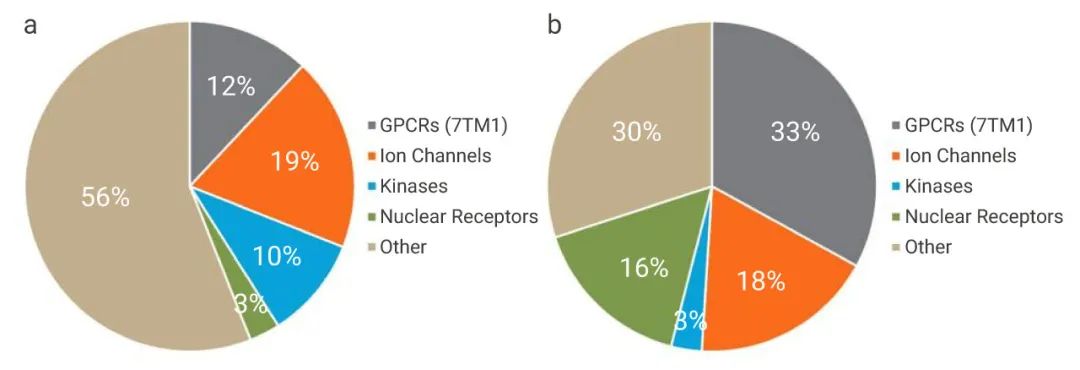
圖 1. 作為藥物靶點的主要蛋白質家族
a. 人類藥物靶點按基因家族分布; b. 這些家族的藥物比例分配
GPCR:G 蛋白偶聯受體,也被稱為七螺旋或 7 次跨膜受體,是人類和許多其他物種中最大的膜受體家族,也是已獲批準藥物的最大靶標蛋白質家族。許多因素促成了 GPCR 靶向藥物的廣泛應用,包括它們的成藥性、與多種類型的化學實體的相互作用以及在質膜中的表達,其膜上的表達促進了細胞外環境中的分子相互作用。GPCR 在糖尿病、肥胖、阿爾茨海默癥和精神疾病等疾病中的重要作用,為持續的藥物發現和開發工作提供很大了動力。
酶:靶向酶是藥物發現和開發的主要焦點之一。酶是生命所有過程中必不可少的生理催化劑,包括新陳代謝、細胞信號傳導和運動,以及細胞生長和分裂。它們是有吸引力的藥物靶標,因為存在確定的底物結合口袋,可用作藥物酶抑制劑的結合位點。James G. Robertson 的文章報道,根據 FDA Orange Book 的分析,市面上有 317 種抑制酶活性的藥物,能抑制 71 種酶,其中包括 48 種人類酶、13 種細菌酶、5 種病毒酶、4 種真菌酶和 1 種原生動物酶。蛋白激酶現已成為僅次于 GPCR 的第二大重要藥物靶標。
藥物研究旨在發現和開發影響疾病相關蛋白質功能或蛋白質-蛋白質相互作用的新化合物,擁有與疾病相關的蛋白質的準確功能和結構信息有助于幫助藥物開發,即藥物靶蛋白需要支持篩選、結構和機制研究,提供驅動化學設計的數據。
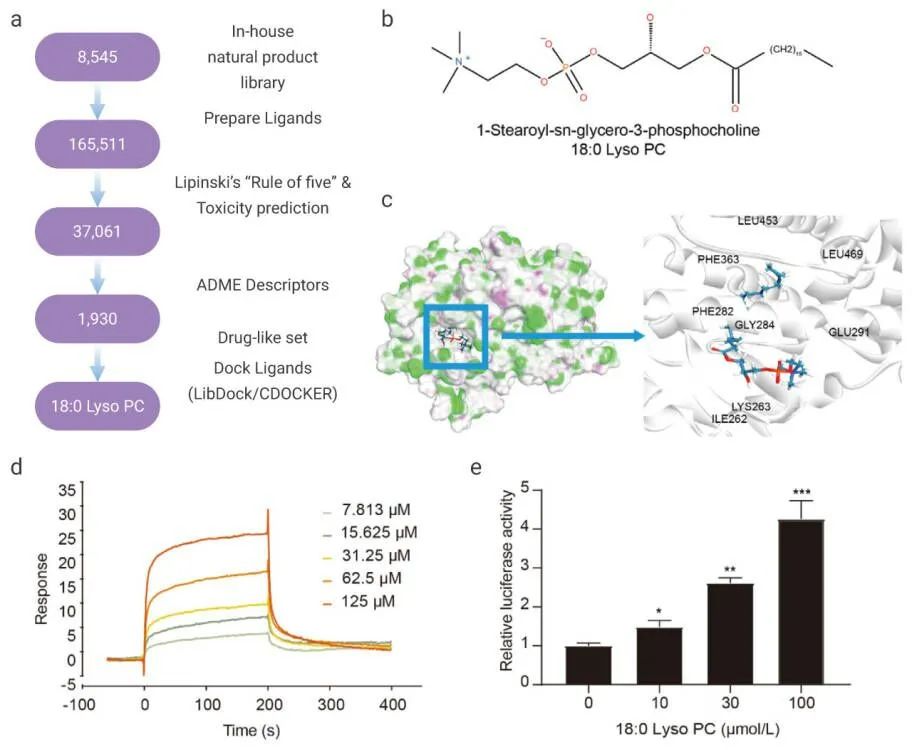
一般來說,結構和基于蛋白質的藥物研究需要大量的蛋白質。例如,晶體學研究至少需要 1 mg 蛋白質。從天然有機來源或通過化學合成幾乎不可能獲得足夠數量的高純度目標蛋白;用于藥物發現的蛋白質庫也需要通過 X 射線晶體學和核磁共振仔細分析蛋白質的三級結構,這些技術需要純化的蛋白質樣品,因此,在蛋白質結構生物學研究中,能夠產生大量重組目的蛋白的“重組”方法是不可缺少的。
高純度、高活性的重組蛋白可以幫助疾病研究獲取多樣的定性、定量數據。藥物篩選及優化中,重組蛋白可用于測試藥物能否作用于潛在靶點蛋白。同時,重組蛋白作為原料是生物藥的質量、有效性和安全的重要保障。因此,重組蛋白成為了生命科學基礎研究中的重要科研工具之一。
多種重組蛋白表達方法已被開發用于藥物靶點研究,MCE 提供細菌 (大腸桿菌)、哺乳動物細胞、昆蟲細胞和酵母多種表達系統來源的重組蛋白,涵蓋多同類別產品,如受體蛋白、酶、免疫檢查點蛋白、CAR-T 相關蛋白等藥物靶標蛋白,可應用于蛋白結構、蛋白相互作用、蛋白-小分子相互作用研究、藥物篩選,助力藥物研發!
|
相關產品 |
|
GPCRs 介導細胞對大多數激素、代謝物、細胞因子和神經遞質的反應,因此是藥物發現的“富有成效靶點”。 |
|
核受體是一種重要的轉錄因子,能夠調控細胞核內的基因表達,以響應各種胞外和胞內信號。核受體是藥物發現的理想靶點。 |
|
酶類是在生物系統內發現的生物催化劑,能催化特定的生化過程,它們是有吸引力的藥物靶標 |
|
免疫檢查點蛋白在維持免疫穩態和預防自身免疫中起著重要的免疫調節作用,癌癥的免疫檢查點治療策略包括了靶向這些調控途徑,以恢復免疫細胞的抗腫瘤功能。 |
|
CAR-T 細胞是通過基因工程表達特異性合成抗原受體的 T 細胞,能夠特異性地靶向抗原并殺死腫瘤細胞,靶標抗原的選擇對 CAR-T 細胞的特異性殺傷作用至關重要。MCE 重組蛋白已覆蓋 BCMA、EGFR、HER2、CD22、CD19、CD138 等 40+ 個 CAR-T 熱門靶標。 |
注:
1、每個庫中的分子數量實時變動,以上分子數量僅供參考,以官網實時數據為準。
2、更多數據庫詳見 MCE 官網。
參考文獻
1. Rita Santos, John P. Overington, Bissan Al-Lazikani, Anne Hersey, Tudor I. Oprea, et al. A comprehensive map of molecular drug targets. Nat Rev Drug Discov. 2017 Jan; 16(1): 19–34.
2. Krishna Sriram, Paul A. Insel. G Protein-Coupled Receptors as Targets for Approved Drugs: How Many Targets and How Many Drugs? Mol Pharmacol. 2018 Apr; 93(4): 251–258.
3. Alexander S. Hauser, David E. Gloriam, et al. Trends in GPCR drug discovery: new agents, targets and indications. Nat Rev Drug Discov. 2017 Dec 1; 16(12): 829–842.
4. Arne ChristianRufer. Drug discovery for enzymes. Drug Discov Today. 2021 Apr;26(4):875-886.
5. James G. Robertson. Mechanistic Basis of Enzyme-Targeted Drugs.Biochemistry 2005, 44, 15, 5561–5571.
6. Philip Cohen. Protein kinases--the major drug targets of the twenty-first century? Nat Rev Drug Discov. 2002 Apr;1(4):309-15.
7. Toshihiko Sugiki, et al. Latest approaches for efficient protein production in drug discovery. Expert Opin Drug Discov. 2014 Oct;9(10):1189-204.
8. Yiming Ma, Chengyu Jiang, et al. 18:0 Lyso PC, a natural product with potential PPAR- g agonistic activity, plays hypoglycemic effect with lower liver toxicity and cardiotoxicity in db/db mice. Biochemical and Biophysical Research Communications, Volume 579, 2021, Pages 168-174.